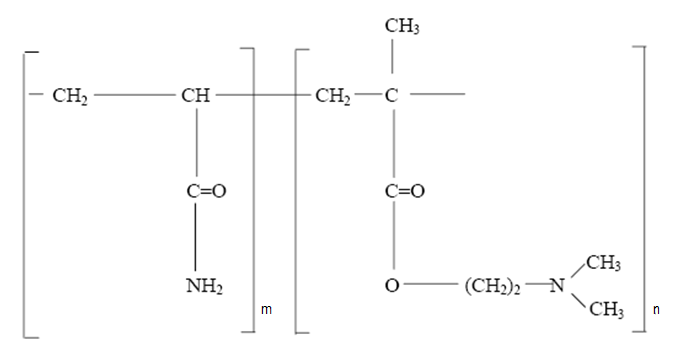
2.1. Consideraţii teoretice
Apa tratată pentru a fi utilizată ca apă potabilă trebuie să respecte directiva 98/83/EC pentru apa potabilă a Consiliului Europei.
Apa este un element esenţial pentru viaţa şi procesele naturale. Are două dimensiuni ce sunt strâns legate – cantitatea şi calitatea. Calitatea apei este asigurată prin caracteristicile sale fizice, chimice, biologice si estetice (aspect şi miros). După provenienţa sursei de apă, se identifică surse de suprafaţă (râuri, lacuri, apa mărilor şi a oceanelor) şi surse de adâncime (apa provenită din pânza freatică)[1].
Conform Normelor tehnice de protecţie a apelor (NTPA) 013/2002, sursele de apă se clasifică funcţie de calitatea şi utilizarea lor în următoarele categorii[2]:
Categoria I: ape destinate alimentărilor cu apăîn sistem centralizat a aglomerărilor urbane, unităţilor cu profil alimentar, industriei farmaceutice, amenajări piscicole.
Categoria II: ape destinate pentru industrie, urbanism, irigaţii.
Categoria III: apa brută netratată utilizatăîn transport.
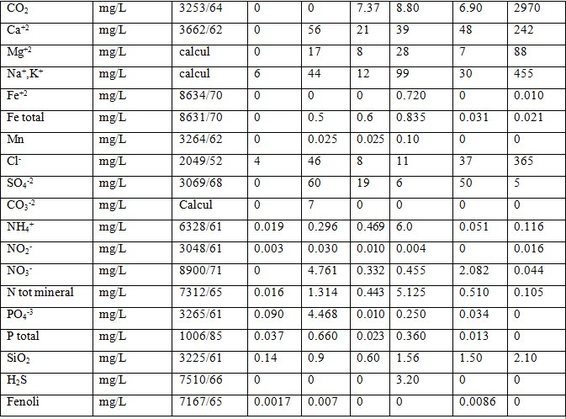
În tabelul 2 sunt menţionaţi indicatorii de calitate pentru diferite categorii de apă[1].
Apa este un element esenţial pentru viaţa şi procesele naturale. Are două dimensiuni ce sunt strâns legate – cantitatea şi calitatea. Calitatea apei este asigurată prin caracteristicile sale fizice, chimice, biologice si estetice (aspect şi miros). După provenienţa sursei de apă, se identifică surse de suprafaţă (râuri, lacuri, apa mărilor şi a oceanelor) şi surse de adâncime (apa provenită din pânza freatică)[1].
Conform Normelor tehnice de protecţie a apelor (NTPA) 013/2002, sursele de apă se clasifică funcţie de calitatea şi utilizarea lor în următoarele categorii[2]:
Categoria I: ape destinate alimentărilor cu apăîn sistem centralizat a aglomerărilor urbane, unităţilor cu profil alimentar, industriei farmaceutice, amenajări piscicole.
Categoria II: ape destinate pentru industrie, urbanism, irigaţii.
Categoria III: apa brută netratată utilizatăîn transport.
În tabelul 2 sunt menţionaţi indicatorii de calitate pentru diferite categorii de apă[1].
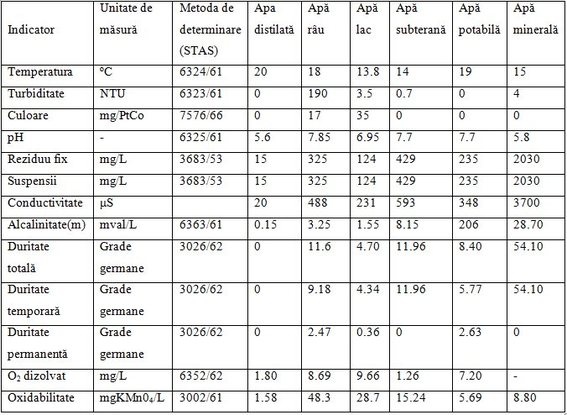
Tabel 2. Indicatori de calitate pentru diferite tipuri de apă
Compararea valorilor indicilor de calitate permite evidenţierea specificului diferitelor categorii de apăşi duce la concluzia că tehnologiile de obţinere a apei potabile trebuie adaptate caracteristicilor şi specificului sursei utilizate.
2.1.1 mETODE DE INVESTIGARE A RESURSELOR DE APA
Calitatea apei nu rămâne constantă în timp, ea poate varia din cauza multor factori fie produşi de om (factori antropici), fie de origine naturală. Analizele chimice reflectă starea momentană a apei[3].Oricât de mare ar fi frecvenţa de analiză a parametrilor gradul avansat al preciziei determinărilor, acestea furnizează informaţii orientative[4].Tipul şi frecvenţa de ritmicitate a analizelor fizico-chimice sunt reglementate de normativul NTPA 014[5].
În practică se determină indicatorii chimici specifici prezentaţi în tabelul 3.
În practică se determină indicatorii chimici specifici prezentaţi în tabelul 3.
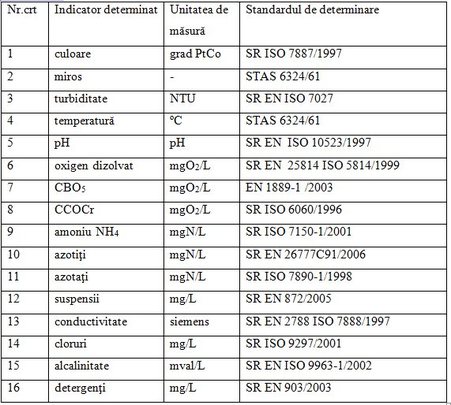
Tabel 3. Indicatorii de bază pentru calitatea apei potabile
Analizele care stabilesc calitatea apei sunt redate mai jos:
- Determinarea temperaturii conform STAS 6324/61. Determinarea temperaturii se realizează direct la sursa de apă, dacă condiţiile de teren o permit. În cazul în care acest lucru nu este posibil, se prelevează o probă de 1-1,5 L de apă şi se decelează temperatura imediat după recoltare. Pentru determinare se folosesc termometre cu mercur sau cu semiconductor.
- Determinarea pH-lui conform SR ISO 10523/1997. Determinarea pH-lui se realizează prin procedeu electrochimic şi constăîn măsurarea forţei electromotoare a unei celule conductometrice alcătuită dintr-un electrod de sticlăşi unul de referinţă. Metoda este aplicabilă tuturor probelor de apă cu pH-ul cuprins între 3–10.
- Determinarea continutului de oxigen dizolvat conform SR EN 25814 ISO 5814/1999 Determinarea conţinutului de oxigen se realizează prin metoda electrochimică cu ajutorul unei celule electrochimice ce comunică cu proba printr-o membrană semipermiabilă la gaz.
- Determinarea consumului biochimic de oxigen dupa n zile (CBO5) conform SR EN 1889-1 /2003. Consumul biochimic de oxigen reprezinta cantitatea de oxigen consumata de microorganisme intr-un interval de timp, pentru descompunerea biochimica a substantelor organice continute in apa. Timpul standard este de cinci zile la temperatura de 20°C.
- Determinarea consumului chimic de oxigen CCOCr conform SR ISO 6060/1996.Consumul chimic de oxigen se defineşte ca fiind concentraţia masică de oxigen, echivalentă cu cantitatea de dicromat de potasiu consumată de materiile dizolvate şi aflate în suspensie.
- Determinarea conţinutului de amoniu conform SR ISO 7150-1 /2001. Determinarea amoniului în apă se realizează pe cale spectrofotometrică, prin reacţia ionului amoniu cu ionii de salicilat şi hipoclorit în prezenţa nitrozo-pentacianoferatului III de sodiu.
- Determinarea continutului de nitriţi conform SR EN 26777C91/2006. Se realizează pe cale spectrală, cu ajutorul unui spectrofotometru cu absorbţie atomică pentru concentraţii de nitriţi de până la 0.25mg/L. Principiul metodei constăîn reacţia ionilor nitrit cu reactivul 4-aminobenzen-sulfonamida în prezenţa acidului ortofosforic pentru a rezulta o sare de diazoniu, care formează un complex de culoare roşie cu N(1-naftil)-etilen–diamina diclorhidrat. Se măsoară apoi absorbanţa la 540 nm.
- Determinarea conținutului de azotaţi conform SR ISO 7890-1/1998se realizează pe cale spectrometrică, pe baza reacţiilor între 2,6-dimetilfenol şi acidul sulfuric, având ca produs de reacţie 4–nitrozo-2,6-dimetilfenol. Măsurarea spectrofotometrică se realizează la lungimea de undă de 324 nm.
- Determinarea suspensiilor conform SR EN 872/2005 Determinarea suspensiilor solide din apa se realizează prin metoda filtrării pe creuzete filtrante sub presiune sau sub vid.
- Determinarea conductivității electrice conform SR EN 2788 ISO7888/1997.Conductivitatea electrică este măsura curentului condus de ionii prezenţi în apăşi depinde de concentraţia lor, temperatura soluţiei şi de viscozitate. Dispozitivul utilizat în determinări se numeşte conductometru şi exprimă acest parametru în micro–Siemens (μS).
- Determinarea conţinutului de cloruri conform SR ISO 9297/2001.Determinarea utilizează metoda Mohr, pe principiul precipitării ionilor de argint cu ionii clorură, adăugarea unui mic exces de ioni de argint şi formarea cromatului de argint cu ionii cromat drept indicator.
-Determinarea alcalinităţii totale şi permanente a apei conformSR EN ISO 9963-1/2002.Alcalinitatea (A) se defineşte ca fiind capacitatea cantitativă a mediilor apoase de a reacţiona cu ionii de hidrogen. Alcalinitatea la punctul de viraj al roşului de metil este o măsură arbitrară a alcalinităţii totale(AT) a apei care se obţine prin titrare până la virajul roşului de metil (pH=4.5). Alcalinitatea la punctul de viraj al fenolftaleinei (alcalinitatea permanentă) (AP) se atribuie arbitrar la măsurarea prin titrare până la punctul de viraj al fenolftaleinei (pH=8.3) şi reprezintă alcalinitatea unei ape corespunzătoare totalităţii hidroxizilor şi jumatate din conţinutul de carbonaţi.
- Determinarea agenţilor de suprafaţă anionici conform SR EN 903/2003.
Metoda se bazează pe determinarea indicelui de albastru de metilen (MBAS), utilizând un spectrofotometru cu selector pentru variatie discontinuă. Principiul constăîn formarea în mediu alcalin a sărurilor colorate dintre albastru de metilen şi agenţii de suprafaţă anionici, extracţia acestor săruri cu cloroform şi tratarea acidă a soluţiei cloroformice, eliminarea complexului, substanţa anionică-albastru de metil, din soluţia alcalinăşi agitarea extractului cu soluţie acidă de albastru de metilen.
- Determinarea temperaturii conform STAS 6324/61. Determinarea temperaturii se realizează direct la sursa de apă, dacă condiţiile de teren o permit. În cazul în care acest lucru nu este posibil, se prelevează o probă de 1-1,5 L de apă şi se decelează temperatura imediat după recoltare. Pentru determinare se folosesc termometre cu mercur sau cu semiconductor.
- Determinarea pH-lui conform SR ISO 10523/1997. Determinarea pH-lui se realizează prin procedeu electrochimic şi constăîn măsurarea forţei electromotoare a unei celule conductometrice alcătuită dintr-un electrod de sticlăşi unul de referinţă. Metoda este aplicabilă tuturor probelor de apă cu pH-ul cuprins între 3–10.
- Determinarea continutului de oxigen dizolvat conform SR EN 25814 ISO 5814/1999 Determinarea conţinutului de oxigen se realizează prin metoda electrochimică cu ajutorul unei celule electrochimice ce comunică cu proba printr-o membrană semipermiabilă la gaz.
- Determinarea consumului biochimic de oxigen dupa n zile (CBO5) conform SR EN 1889-1 /2003. Consumul biochimic de oxigen reprezinta cantitatea de oxigen consumata de microorganisme intr-un interval de timp, pentru descompunerea biochimica a substantelor organice continute in apa. Timpul standard este de cinci zile la temperatura de 20°C.
- Determinarea consumului chimic de oxigen CCOCr conform SR ISO 6060/1996.Consumul chimic de oxigen se defineşte ca fiind concentraţia masică de oxigen, echivalentă cu cantitatea de dicromat de potasiu consumată de materiile dizolvate şi aflate în suspensie.
- Determinarea conţinutului de amoniu conform SR ISO 7150-1 /2001. Determinarea amoniului în apă se realizează pe cale spectrofotometrică, prin reacţia ionului amoniu cu ionii de salicilat şi hipoclorit în prezenţa nitrozo-pentacianoferatului III de sodiu.
- Determinarea continutului de nitriţi conform SR EN 26777C91/2006. Se realizează pe cale spectrală, cu ajutorul unui spectrofotometru cu absorbţie atomică pentru concentraţii de nitriţi de până la 0.25mg/L. Principiul metodei constăîn reacţia ionilor nitrit cu reactivul 4-aminobenzen-sulfonamida în prezenţa acidului ortofosforic pentru a rezulta o sare de diazoniu, care formează un complex de culoare roşie cu N(1-naftil)-etilen–diamina diclorhidrat. Se măsoară apoi absorbanţa la 540 nm.
- Determinarea conținutului de azotaţi conform SR ISO 7890-1/1998se realizează pe cale spectrometrică, pe baza reacţiilor între 2,6-dimetilfenol şi acidul sulfuric, având ca produs de reacţie 4–nitrozo-2,6-dimetilfenol. Măsurarea spectrofotometrică se realizează la lungimea de undă de 324 nm.
- Determinarea suspensiilor conform SR EN 872/2005 Determinarea suspensiilor solide din apa se realizează prin metoda filtrării pe creuzete filtrante sub presiune sau sub vid.
- Determinarea conductivității electrice conform SR EN 2788 ISO7888/1997.Conductivitatea electrică este măsura curentului condus de ionii prezenţi în apăşi depinde de concentraţia lor, temperatura soluţiei şi de viscozitate. Dispozitivul utilizat în determinări se numeşte conductometru şi exprimă acest parametru în micro–Siemens (μS).
- Determinarea conţinutului de cloruri conform SR ISO 9297/2001.Determinarea utilizează metoda Mohr, pe principiul precipitării ionilor de argint cu ionii clorură, adăugarea unui mic exces de ioni de argint şi formarea cromatului de argint cu ionii cromat drept indicator.
-Determinarea alcalinităţii totale şi permanente a apei conformSR EN ISO 9963-1/2002.Alcalinitatea (A) se defineşte ca fiind capacitatea cantitativă a mediilor apoase de a reacţiona cu ionii de hidrogen. Alcalinitatea la punctul de viraj al roşului de metil este o măsură arbitrară a alcalinităţii totale(AT) a apei care se obţine prin titrare până la virajul roşului de metil (pH=4.5). Alcalinitatea la punctul de viraj al fenolftaleinei (alcalinitatea permanentă) (AP) se atribuie arbitrar la măsurarea prin titrare până la punctul de viraj al fenolftaleinei (pH=8.3) şi reprezintă alcalinitatea unei ape corespunzătoare totalităţii hidroxizilor şi jumatate din conţinutul de carbonaţi.
- Determinarea agenţilor de suprafaţă anionici conform SR EN 903/2003.
Metoda se bazează pe determinarea indicelui de albastru de metilen (MBAS), utilizând un spectrofotometru cu selector pentru variatie discontinuă. Principiul constăîn formarea în mediu alcalin a sărurilor colorate dintre albastru de metilen şi agenţii de suprafaţă anionici, extracţia acestor săruri cu cloroform şi tratarea acidă a soluţiei cloroformice, eliminarea complexului, substanţa anionică-albastru de metil, din soluţia alcalinăşi agitarea extractului cu soluţie acidă de albastru de metilen.
2.1.2. Compoziţia fizico-chimică şi calitatea apei
Compoziţia şi calitatea apelor naturale este determinată de totalitatea substanţelor minerale şi organice, a gazelor dizolvate, a particulelor aflate sub formă de suspensii şi a organismelor vii prezente[6].
În România indicatorii de calitate sunt evaluaţi de STAS 1342/1991[7]şi legea 458/2002 [8] modificatăşi completată cu 311/2004 [9](legea calităţii apei în România).
Indicatori organoleptici şi fizici:
Culoarea apelor se datorează substanţelor dizolvate şi se determinăîn comparaţie cu etaloane preparate în laborator sau în raport cu apa bidistilată, unitatea de măsură fiind gradul platino-cobalt.
Mirosul apei se clasifică în:fără miros, cu miros neperceptibil, cu miros perceptibil unui specialist, cu miros perceptibil unui consumator, cu miros puternic şi cu miros foarte puternic.
Gustul apei se clasifică utilizându-se denumiri convenţionale cum ar fi:
Mb - ape cu gust mineral bicarbonato-sodic; Mg - ape cu gust magnezic; Mn – ape cu gust mineral metalic; Ms - ape cu gust mineral sărat; Oh – ape cu gust organic hidrocarbonat; Om - ape cu gust organic pământos; Ov - ape cu gust organic gazos.
Turbiditatea apei se manifestă prin lipsa de transparenţă a acesteia şi se datorează prezenţei substanţelor în suspensie fin divizate (argilă, nisip, substanţă organică ) care impiedică razele de lumină să se propage liber. Acestea se pot separa prin metode fizice: filtrare, centrifugare, sedimentare. Turbiditatea apei se determină pe cale optică cu un dispozitiv numit turbidimetru, cu ajutorul căruia se măsoară transparenţa probei în raport cu un etalon pe bază de formazină. Unitatea de măsură este gradul NTU sau NFU (grade nefelometrice de turbiditate).
pH-ul - reprezintă un factor important care determină capacitatea de reactivitate a apei, agresivitatea acesteia, capacitatea de a constitui medii pentru dezvoltarea diferitelor organisme.
Conductivitatea apelor constituie unul din indicatorii cei mai utilizaţi în aprecierea gradului de mineralizare a apelor. Conductivitatea electrică este influenţată în mod direct de concentraţia totală a ionilor în apă (cationic şi anionic). Unitatea de măsură este Ω-1.cm-1. Dispozitivul de măsură este un conductometru bazat pe o punte Wheatstone.
Radioactivitatea apei - reprezintă capacitatea acesteia de a emite radiaţii permanente de tip: alfa, beta şi gamma. Substanţele radioactive induc prin expunere îndelungatăşi la nivele ridicate, mutaţii genetice ireversibile şi boli de radiaţie, deobicei letale. Acestea nu pot fi utilizate în scopuri de alimentare casnicăşi industrială.
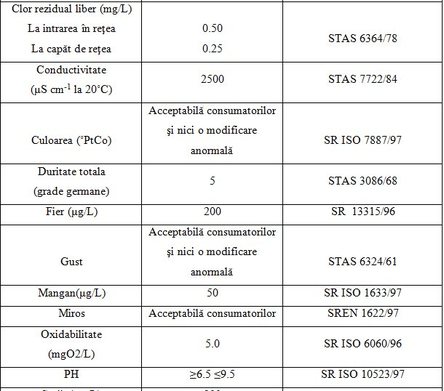
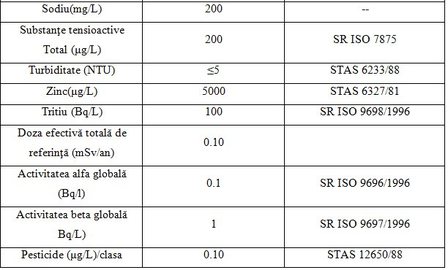
Indicatori chimici Cei mai importanţi indicatori chimici generali specificaţi în legea calităţii apei din România [14,15], sunt redaţi în tabelul 4.
În România indicatorii de calitate sunt evaluaţi de STAS 1342/1991[7]şi legea 458/2002 [8] modificatăşi completată cu 311/2004 [9](legea calităţii apei în România).
Indicatori organoleptici şi fizici:
Culoarea apelor se datorează substanţelor dizolvate şi se determinăîn comparaţie cu etaloane preparate în laborator sau în raport cu apa bidistilată, unitatea de măsură fiind gradul platino-cobalt.
Mirosul apei se clasifică în:fără miros, cu miros neperceptibil, cu miros perceptibil unui specialist, cu miros perceptibil unui consumator, cu miros puternic şi cu miros foarte puternic.
Gustul apei se clasifică utilizându-se denumiri convenţionale cum ar fi:
Mb - ape cu gust mineral bicarbonato-sodic; Mg - ape cu gust magnezic; Mn – ape cu gust mineral metalic; Ms - ape cu gust mineral sărat; Oh – ape cu gust organic hidrocarbonat; Om - ape cu gust organic pământos; Ov - ape cu gust organic gazos.
Turbiditatea apei se manifestă prin lipsa de transparenţă a acesteia şi se datorează prezenţei substanţelor în suspensie fin divizate (argilă, nisip, substanţă organică ) care impiedică razele de lumină să se propage liber. Acestea se pot separa prin metode fizice: filtrare, centrifugare, sedimentare. Turbiditatea apei se determină pe cale optică cu un dispozitiv numit turbidimetru, cu ajutorul căruia se măsoară transparenţa probei în raport cu un etalon pe bază de formazină. Unitatea de măsură este gradul NTU sau NFU (grade nefelometrice de turbiditate).
pH-ul - reprezintă un factor important care determină capacitatea de reactivitate a apei, agresivitatea acesteia, capacitatea de a constitui medii pentru dezvoltarea diferitelor organisme.
Conductivitatea apelor constituie unul din indicatorii cei mai utilizaţi în aprecierea gradului de mineralizare a apelor. Conductivitatea electrică este influenţată în mod direct de concentraţia totală a ionilor în apă (cationic şi anionic). Unitatea de măsură este Ω-1.cm-1. Dispozitivul de măsură este un conductometru bazat pe o punte Wheatstone.
Radioactivitatea apei - reprezintă capacitatea acesteia de a emite radiaţii permanente de tip: alfa, beta şi gamma. Substanţele radioactive induc prin expunere îndelungatăşi la nivele ridicate, mutaţii genetice ireversibile şi boli de radiaţie, deobicei letale. Acestea nu pot fi utilizate în scopuri de alimentare casnicăşi industrială.
Indicatori chimici Cei mai importanţi indicatori chimici generali specificaţi în legea calităţii apei din România [14,15], sunt redaţi în tabelul 4.
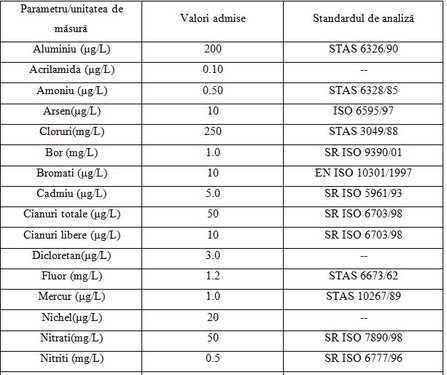
Tabel 4. Indicatori chimici generali şi valorile admise conform legii 458/2002
Indicatori biogeni
Analiza hidrobiologică constă în inventarierea microscopică a fito şi zooplanctonului, organisme din masa apei, precum şi analiza organismelor bentonice (situate pe fundul apei) şi a perifitonului (organisme fixate pe diferite suporturi), din probele de apă prelevate în secţiunea de control.
Analiza bacteriologică a apei urmăreşte numărul total de germeni şi determinarea bacilului E- coli. În tabelul 5 sunt prezentaţi indicatorii biologici, valorile maxime admise şi metoda de analiză[10].
Analiza hidrobiologică constă în inventarierea microscopică a fito şi zooplanctonului, organisme din masa apei, precum şi analiza organismelor bentonice (situate pe fundul apei) şi a perifitonului (organisme fixate pe diferite suporturi), din probele de apă prelevate în secţiunea de control.
Analiza bacteriologică a apei urmăreşte numărul total de germeni şi determinarea bacilului E- coli. În tabelul 5 sunt prezentaţi indicatorii biologici, valorile maxime admise şi metoda de analiză[10].
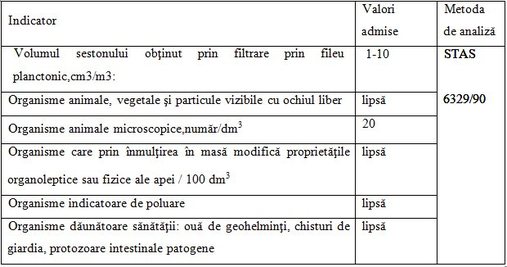
Tabel 5.Indicatori biologici şi valorile admisibile
2.1.3. Tehnici aplicabile în obţinerea apei potabile
În figura 1 este prezent fluxul de tratare a apei dintr-o sursă de adâncime.
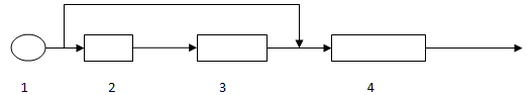
Figura 1.Schema bloc a fluxului de tratare a apei din sursa de adâncime
1- captare din puţ de adâncime, 2-bloc de aerare, 3-filtre rapide cu nisip, 4-sistemul de dezinfecţie( clor gazos, dioxid de clor)
1- captare din puţ de adâncime, 2-bloc de aerare, 3-filtre rapide cu nisip, 4-sistemul de dezinfecţie( clor gazos, dioxid de clor)
În figura 2 este prezentat fluxul de tratare a apelor de suprafaţă(râu sau lac):
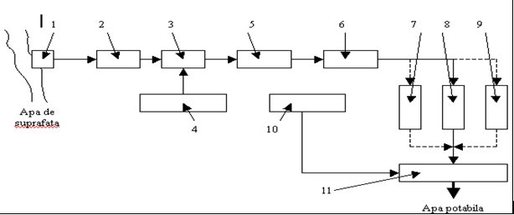
Figura 2. Schema bloc de tratare convenţională a apei din surse de suprafaţă
1-priza de captare, 2-sistemul de admisie a apei, 3-blocul de injecţie a reactivilor de tratare,4-gospodaria de reactivi, 5-tanc de reacţie, 6-decantoare, 7-filtre cu cărbune activat, 8-filtre cu nisip, 9-sisteme de tratare specială a apei (osmoza inversă, dedurizare, oxigenare, deferizare), 10- staţia de clorare (dozare clor, generare şi dozare dioxid de clor), 11-rezervorul de apă potabilă.
1-priza de captare, 2-sistemul de admisie a apei, 3-blocul de injecţie a reactivilor de tratare,4-gospodaria de reactivi, 5-tanc de reacţie, 6-decantoare, 7-filtre cu cărbune activat, 8-filtre cu nisip, 9-sisteme de tratare specială a apei (osmoza inversă, dedurizare, oxigenare, deferizare), 10- staţia de clorare (dozare clor, generare şi dozare dioxid de clor), 11-rezervorul de apă potabilă.
2.1.3.1. Sisteme de reţinere a particulelor grosiere
În scopul protejării mecanice a instalaţiilor de tratare, de obiectele plutitoare antrenate de apele de suprafaţă (corpuri plutitoare, resturi vegetale şi animale), în punctele de captare a apei brute, se dispun grătare şi site.Grătarele servesc pentru îndepărtarea din apă a impurităţilor grosiere care pot forma depuneri greu de evacuat şi care ar bloca utilajele.Materialele reţinute, cu dimensiuni mai mari decât interstiţiile dintre bare, formează ele însele straturi filtrante. Pentru reţinerea impurităţilor de dimensiuni mai mici se utilizează site statice sau mobile. Deznisiparea are ca scop reţinerea în bazine special amenajate a nisipului şi reprezintă prima treaptă de limpezire în procesul de tratare a apei [13,14].
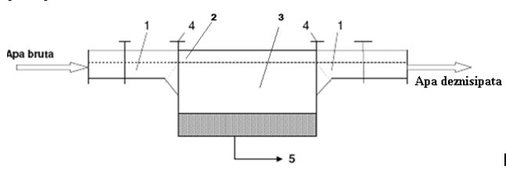
Figura 3. Deznisipator orizontal
1- camera de liniştire, 2-grătare pentru reţinerea suspensiilor plutitoare grosiere, 3-camera de sedimentare, 4-praguri, stavilare, 5-dispozitive de evacuare a nisipului.
1- camera de liniştire, 2-grătare pentru reţinerea suspensiilor plutitoare grosiere, 3-camera de sedimentare, 4-praguri, stavilare, 5-dispozitive de evacuare a nisipului.
2.1.3.2. Coagularea – flocularea
Dimensiunea impurităţilordin apa brută variază de la 10-7mm la circa 1 mm. O parte din aceste particule pot fi separate prin sedimentare, iar o altă parte din impurităţi având dimensiuni şi viteze de sedimentare prea mici nu pot fi separate din apă pe această cale[15]. Din acest motiv este nevoie să se recurgă la agregarea lor în particule mai mari, ce pot fi îndepărtate prin coagulare şi sedimentare. Particulele foarte fine sunt incărcate electric şi se resping între ele[13, 16].
Conform concepţiei stratului dublu electric există un strat de adsorbţie, care aderă direct la nucleu, denumit „strat fix” sau „Helmholtz”şi un strat difuz, care este format din contraioni. Schema unei particule coloidale este prezentata in figura 11. Particulele coloidale din apa, încărcate negativ, au potenţial, numit potential „ZETA”[13,17,18]. Valorea potenţialului Zeta a apelor din Romania se situeazăîn intervalul: -10mV si -30 mV. Coloizii fiind încărcaţi negativ, aceasta le conferă stabilitate, nu sedimentează şi se menţin în echilibru mult timp. Destabilizarea echilibrului coloidal se realizează prin neutralizarea sarcinilor electrice ce conduce la formarea unor particule mai mari, denumite „flocoane”capabile să sedimenteze.
Conform concepţiei stratului dublu electric există un strat de adsorbţie, care aderă direct la nucleu, denumit „strat fix” sau „Helmholtz”şi un strat difuz, care este format din contraioni. Schema unei particule coloidale este prezentata in figura 11. Particulele coloidale din apa, încărcate negativ, au potenţial, numit potential „ZETA”[13,17,18]. Valorea potenţialului Zeta a apelor din Romania se situeazăîn intervalul: -10mV si -30 mV. Coloizii fiind încărcaţi negativ, aceasta le conferă stabilitate, nu sedimentează şi se menţin în echilibru mult timp. Destabilizarea echilibrului coloidal se realizează prin neutralizarea sarcinilor electrice ce conduce la formarea unor particule mai mari, denumite „flocoane”capabile să sedimenteze.
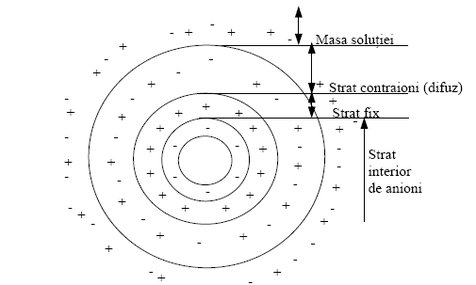
Figura 4. Modelul stratului dublu electric
Destabilizarea coloizilor se poate realiza prin tratarea apei cu ioni metalici, eficienţa sporind cu creşterea valenţei ionilor metalici. În practică se folosesc sărurile de metale trivalente pe bază de Fe(III) şi Al(III)[13,19,20]. Se remarcă clorura ferică şi sulfatul de aluminiu.
Reactivul pe bază de fer(III) cel mai utilizat în tratarea apelor de suprafaţăîl constituieFeCl3⋅6H2O, ce se prezintă sub formă de cristale brune, foarte higroscopice, în practică utilizându-se sub formă de soluţie concentrată (40%).
Reacţia de hidroliză a FeCl3în prezenţa HCO-3 din apa brută este:
FeCl3 + HCO3- ↔ Fe (OH)3 ↓ + 3Cl- + 3CO2 (1)
Reactivul pe bază de fer(III) cel mai utilizat în tratarea apelor de suprafaţăîl constituieFeCl3⋅6H2O, ce se prezintă sub formă de cristale brune, foarte higroscopice, în practică utilizându-se sub formă de soluţie concentrată (40%).
Reacţia de hidroliză a FeCl3în prezenţa HCO-3 din apa brută este:
FeCl3 + HCO3- ↔ Fe (OH)3 ↓ + 3Cl- + 3CO2 (1)
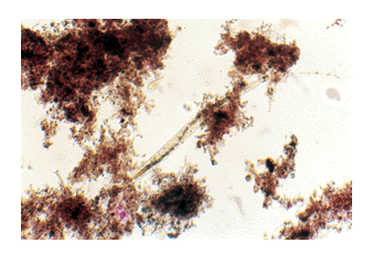
Figura 5. Flocoane formate în tancul de reacţie, utilizând reactiv de coagulare FeCl3,în Complexul de Tratarea Apei Chiriţa Iaşi
În noua tehnologie au fost înlocuiţi unii reactivi de tratare: s-a renunţat complet la utilizarea sulfatului de aluminiu (Al2(SO4)3, acesta fiind implicat în declanşarea sindromului Allzenheimer, înlocuindu-se cu clorura ferică (FeCl3) .
Agenţii de floculare, substanţe cunoscute şi sub denumirea de adjuvanţi, sunt utilizaţi în procesul de coagulare-floculare, cu scopul de a realiza o mărire a dimensiunilor flocoanelor şi a vitezei de sedimentare. Adjuvanţii utilizaţi în coagulare-floculare sunt de origine minerală sau de origine organică[21].Adjuvanţi minerali, din această grupă fac parte: silicea activă (silicat de sodiu neutralizat cu H2SO4), silico-aluminat (silicat de sodiu activat cu sulfat de aluminiu), argile (bentonita, caolin), nisip fin, cărbune activ, carbonat de calciu, kiselgur.
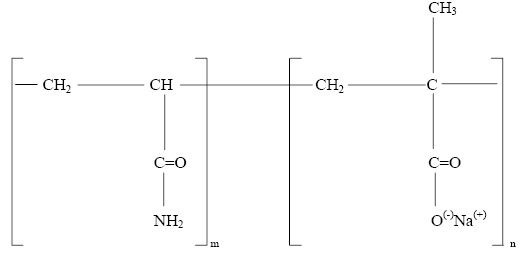
Adjuvanţi organici de sinteză, [13,21,22]sunt macromolecule cu catene lungi, obţinute prin asocierea monomerilor sintetici, având sarcini electrice sau grupe ionizabile. Aceşti compuşi cu diferite valori pentru masa moleculara prezintă eficienţă superioară polimerilor naturali şi se clasificăîn trei grupe:
- neutri(neionici) de tip poliacrilamidă, cu cea mai mare aplicabilitate practică,
- anionici, de tip copolimeri ai acrilamidei cu acid acrilic.
Agenţii de floculare, substanţe cunoscute şi sub denumirea de adjuvanţi, sunt utilizaţi în procesul de coagulare-floculare, cu scopul de a realiza o mărire a dimensiunilor flocoanelor şi a vitezei de sedimentare. Adjuvanţii utilizaţi în coagulare-floculare sunt de origine minerală sau de origine organică[21].Adjuvanţi minerali, din această grupă fac parte: silicea activă (silicat de sodiu neutralizat cu H2SO4), silico-aluminat (silicat de sodiu activat cu sulfat de aluminiu), argile (bentonita, caolin), nisip fin, cărbune activ, carbonat de calciu, kiselgur.
Adjuvanţi organici de sinteză, [13,21,22]sunt macromolecule cu catene lungi, obţinute prin asocierea monomerilor sintetici, având sarcini electrice sau grupe ionizabile. Aceşti compuşi cu diferite valori pentru masa moleculara prezintă eficienţă superioară polimerilor naturali şi se clasificăîn trei grupe:
- neutri(neionici) de tip poliacrilamidă, cu cea mai mare aplicabilitate practică,
- anionici, de tip copolimeri ai acrilamidei cu acid acrilic.
- cationici,de tip copolimeri ai acrilamidei cu un monomer cationic. Exemplu: metacrilat de dimetilamino-etil.
Pentru ca reactivul de coagulare-floculare introdus în apă să aibă eficacitatea necesară, acesta trebuie amestecat rapid şi perfect cu apa brută[12,13,23]. În acest scop se folosesc camerele de amestec.
În figurile 6şi 7 sunt prezentate sistemele de stocare şi dozare a reactivului de coagulare, integrate în Complexul Chiriţa.
În figurile 6şi 7 sunt prezentate sistemele de stocare şi dozare a reactivului de coagulare, integrate în Complexul Chiriţa.

Figura 6. Sistem de rezervoare pentru stocarea reactivului de coagulare

Figura 7.Sistem automat Alldos pentru dozarea clorurii ferice
Reactivul utilizat pentru floculare în tehnologia de tratare a apei din sursa Prut este poliacrilamida.
Decantarea apei este un proces de separare (solid-lichid), bazat pe sedimentarea fazei cu densitate superioară sub acţiunea câmpului gravitaţional [13, 24-26]. Lichidul limpede ce rezultă după decantare poartă denumirea de decantat. Separarea gravitaţională se bazează pe faptul că asupra unui corp aflat în câmp gravitaţional acţionează o forţă, ce determină deplasarea corpului spre fundul bazinului de separare Fg şi de forţa de frecare între particule ce sedimenteazăşi mediu (apă) în care are loc procesul de sedimentare Ff. Aceste forţe sunt descrise prin ecuaţiile (1) şi (2):
Decantarea apei este un proces de separare (solid-lichid), bazat pe sedimentarea fazei cu densitate superioară sub acţiunea câmpului gravitaţional [13, 24-26]. Lichidul limpede ce rezultă după decantare poartă denumirea de decantat. Separarea gravitaţională se bazează pe faptul că asupra unui corp aflat în câmp gravitaţional acţionează o forţă, ce determină deplasarea corpului spre fundul bazinului de separare Fg şi de forţa de frecare între particule ce sedimenteazăşi mediu (apă) în care are loc procesul de sedimentare Ff. Aceste forţe sunt descrise prin ecuaţiile (1) şi (2):
unde:
ρ1, ρ2: densitatile particulei şi a fluidului
d, V: diametrulşi volumul particulei
v: viteza de depunere a particulei
g: acceleraţia gravitaţională
C: coeficientul de rezistenţă a mediului
Sedimentarea particulelor într-un bazin rectangular ideal este prezentată în figura 8, unde se pot observa traiectoriile teoretice (traiectorii drepte) şi cele întâlnite în practică (traiectorii curbe):
ρ1, ρ2: densitatile particulei şi a fluidului
d, V: diametrulşi volumul particulei
v: viteza de depunere a particulei
g: acceleraţia gravitaţională
C: coeficientul de rezistenţă a mediului
Sedimentarea particulelor într-un bazin rectangular ideal este prezentată în figura 8, unde se pot observa traiectoriile teoretice (traiectorii drepte) şi cele întâlnite în practică (traiectorii curbe):
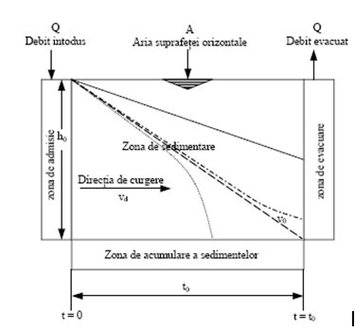
Figura 8. Schema sedimentării în apă a particulelor greu solubile într-un bazin rectangular
În figura 9 este prezentat decantorul suspensional de tip recirculator implementat în fluxul de tratare a apei în Complexul Chiriţa Iaşi[12].

Figura 9. Decantor suspensional integrat în fluxul de tratare a apei din Complexul Chiriţa Iaşi
Flocoanele realizate se depun gravitational pe fundul decantorului, fiind dirijate de podul raclor spre vasele de evacuare. Apa limpezită este colectată şi trimisă gravitaţional spre sistemul filtrelor cu nisip, unde are loc separarea avansată a impurităţilor din apă.
Apa filtrată este colectată într-un rezervor, unde se aplică tehnica oxidării intermediare, cu dioxid de clor, pentru a reduce substanţa organică.
Apa filtrată este colectată într-un rezervor, unde se aplică tehnica oxidării intermediare, cu dioxid de clor, pentru a reduce substanţa organică.
2.1.3.3. Filtrarea apei
Filtrarea constituie procedeul de limpezire avansată a apei, constând în trecerea acesteia printr-o masă de material poros denumit strat filtrant[13]. Filtrarea este utilizată ca ultimă etapă de limpezire în procesul de obţinere a apei potabile. Stratul filtrant poate fi caracterizat ca strat granular sau strat poros. Filtrele din materiale granulare se clasifică după natura materialului filtratant ce poate fi : nisip cuarţos, antracit, cărbune activ granular, cocs metalurgic.
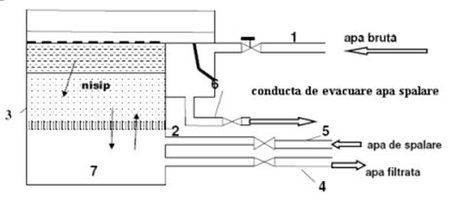
Figura 10. Schema funcţională a unui filtru rapid deschis
1-conducta de alimentare cu apa brută, 2- strat drenant care susţine stratul de nisip, 3- strat de nisip filtrant,4-conducta de evacuare a apei filtrate.
1-conducta de alimentare cu apa brută, 2- strat drenant care susţine stratul de nisip, 3- strat de nisip filtrant,4-conducta de evacuare a apei filtrate.
În figura 11 este prezentat un filtru de tip deschis, integrat în fluxul de tratare a apei din Complexul de Tratare a Apei Chiriţa Iaşi [12] .

Figura 11. Sala cu filtre rapide de tip deschis din Complexul Chiriţa Iaşi
Tehnica filtrării prin cărbune activ granular
Cărbunele activ este un material solid, pe bază de cărbune amorf, cu suprafaţa specifică şi o capacitate de absorbţie deosebit de mare [27]. Calitatea cărbunelui activ este exprimată prin parametrul: “indice de iod” (Iodine #), acesta fiind o măsură a cantităţii de iodură absorbită de cărbunele activ, în unităţi de greutate. Materia primă din care se obţine cărbunele activ performant poate fi coaja de nucă de cocos, lemn (mangal), lignit, turbă, deşeuri petroliere, care prin carbonizare lentă în absenţa aerului şi activare prin injectarea de gaze oxidante la temperaturi foarte înalte conduc la un cărbune activat cu o suprafaţă de adsorbţie ce variază între 500 – 1500 m2/g[28,29]. Injectarea gazului asigură formarea structurii poroase, creând o suprafaţă mare de contact [13]. Cărbunele activ se poate utiliza sub formă de granule (cu spectru granulometric de 2 – 6 mm) în filtre rapide de tip deschis şi sub formă de pulbere sau pudră (cu spectru granulometric 0.1-0.5mm), utilizat sub formă de soluţie de pudră de cărbune activ în procesele de absorbţie chimică şi corectarea parametrilor organoleptici ai apei.
Există mai multe tipuri de adsorbţie ce pot fi luate în consideraţie [13,30]:
- adsorbţie fizică,acumularea poluanţilor realizându-se la zona de separaţie lichid–solid, bazată pe interacţiuni de tip Van der Waals[13,30]
- chemosorbţie, compuşii poluanţi fiind atraşi şi fixaţi numai de centri activi, legături ce implică transfer electronic [13,30]
Adsorbţia combinată cu procesele biologice se realizeazăatunci când căăbunele granular prezintă şi activitate biologică, la suprafaţa granulei creându-se o membrană biologică prin dezvoltarea unor microorganisme ce vor consuma substanţa organică din apă[30,31].
Pe măsură ce cărbunele activ adsoarbe compuşii poluanţi, capacitatea de adsorbţie scade [13], din acest motiv impunându-se regenerarea lui.
Din rezervorul de apă filtrată, apa este preluată de pompele de transfer şi pompată spre filtrele cu cărbune activ. Filtrarea prin bateriile de cărbune activ are ca scop principal corectarea proprietăţilor organoleptice ale apei (gust, culoare, miros, reţinerea ultimilor poluanţi chimici). Cărbunele activ are proprietăţi adsorbante mari, datorită faptului că este în stare granulară, iar suprafaţa specifică este mare. La interfaţa de separaţie apă-suprafaţa granulei se creează o membrană microbiologică, în care se desfăşoară practic fenomenele de adsorbţie biochimică.
Există mai multe tipuri de adsorbţie ce pot fi luate în consideraţie [13,30]:
- adsorbţie fizică,acumularea poluanţilor realizându-se la zona de separaţie lichid–solid, bazată pe interacţiuni de tip Van der Waals[13,30]
- chemosorbţie, compuşii poluanţi fiind atraşi şi fixaţi numai de centri activi, legături ce implică transfer electronic [13,30]
Adsorbţia combinată cu procesele biologice se realizeazăatunci când căăbunele granular prezintă şi activitate biologică, la suprafaţa granulei creându-se o membrană biologică prin dezvoltarea unor microorganisme ce vor consuma substanţa organică din apă[30,31].
Pe măsură ce cărbunele activ adsoarbe compuşii poluanţi, capacitatea de adsorbţie scade [13], din acest motiv impunându-se regenerarea lui.
Din rezervorul de apă filtrată, apa este preluată de pompele de transfer şi pompată spre filtrele cu cărbune activ. Filtrarea prin bateriile de cărbune activ are ca scop principal corectarea proprietăţilor organoleptice ale apei (gust, culoare, miros, reţinerea ultimilor poluanţi chimici). Cărbunele activ are proprietăţi adsorbante mari, datorită faptului că este în stare granulară, iar suprafaţa specifică este mare. La interfaţa de separaţie apă-suprafaţa granulei se creează o membrană microbiologică, în care se desfăşoară practic fenomenele de adsorbţie biochimică.
2.1.3.4. Dezinfecţia apei
Apa brută, până a fi supusă tratării, intrăîn contact cu atmosfera terestră, solul, diferiţi poluanţi, cu o anumităîncărcare microbiologică, existând riscul transmiterii unor boli digestive periculoase pentru sănătatea omului. Din acest motiv se impune distrugerea şi eliminarea acestor microorganisme din apă,prin dezinfecţie cu agenţi chimici puternic oxidanţi sau cu agenţi fizici. Eliminarea totală a agenților patogeni din apă (bacterii, alge, spori, viruşi) se realizează prin sterilizare[13].
Procedeele de dezinfecţie a apei se pot clasifica astfel[13]:
- procedee fizice: ce utilizează anumite forme de energie cu putere de pătrundere mare precum: razele U.V., razele X, razele gamma, câmpul ultrasonic, radiaţia infraroşie, microundele.
- procedee chimice: ce utilizează reactivi chimici puternic oxidanţi precum: clor, dioxid de clor, ozon, apă oxigenată sau ioni ai unor metale grele (argint, cupru).
Procesul de dezinfecţie se realizeazăîn două faze[32]:
- pătrunderea dezinfectantului prin peretele celular
- denaturarea protoplasmei enzimatice
Inactivarea bacteriilor se realizează prin degradarea membranei citoplasmatice şi creşterea permiabilităţii acesteia, urmată de o oxidare a enzimelor implicate în respiraţie. În cazul viruşilor, acţiunea dezinfectantului se manifestă la nivelul acizilor nucleici, în timp ce la protozoare, fenomenele ce au loc sunt mai puţin cunoscute.
Procedeele de dezinfecţie a apei se pot clasifica astfel[13]:
- procedee fizice: ce utilizează anumite forme de energie cu putere de pătrundere mare precum: razele U.V., razele X, razele gamma, câmpul ultrasonic, radiaţia infraroşie, microundele.
- procedee chimice: ce utilizează reactivi chimici puternic oxidanţi precum: clor, dioxid de clor, ozon, apă oxigenată sau ioni ai unor metale grele (argint, cupru).
Procesul de dezinfecţie se realizeazăîn două faze[32]:
- pătrunderea dezinfectantului prin peretele celular
- denaturarea protoplasmei enzimatice
Inactivarea bacteriilor se realizează prin degradarea membranei citoplasmatice şi creşterea permiabilităţii acesteia, urmată de o oxidare a enzimelor implicate în respiraţie. În cazul viruşilor, acţiunea dezinfectantului se manifestă la nivelul acizilor nucleici, în timp ce la protozoare, fenomenele ce au loc sunt mai puţin cunoscute.
2.1.3.4.1. Dezinfecţia prin clorare (cu clor şi derivaţi cloruraţi)
Pentru clorinare se utilizeaza clorul gazos şi substanţele clorigene (clorura de var, cloraminele, dioxidul de clor, hipocloritul de sodiu)[13]. Introdus în apă clorul generează oxigen care acţionează asupra substanţelor organice şi microorganismelor, distrugându-le. În contact cu apa, clorul formează acidul hipocloros şi acidul clorhidric conform reacţiei:
Cl2+H2O → HOCl +HCl (3)
Acidul hipocloros este instabil si se descompune în oxigen activ şi acid clorhidric, conform reacţiei:
HOCl → HCl +O. (4)
Dezavantajul major a dezinfecţiei cu clor gazos o prezintă produşii secundari de reacţie din categoria trihalometanilor (THM), ce rezultăîn urma reacţiei clorului cu substanţele organice din apă, cloroform, diclorometan ( presupuşi a fi agenţi cancerigeni[13,27,33]).
Cloraminele pot fi utilizate în dezinfecţia apei potabile, având efect bactericid mai scăzut decât al clorului. La hiperclorare apar subproduşi de reacţie, precum halometanii, compuşi presupuşi periculoşi [13,34-35].
O alternativă la dezinfecţia cu clor gazos o constituie dioxidul de clor[36], care prezintăproprietăţi specifice: caracter puternic oxidant, capacitate de a reduce, până la eliminarea totalăa ionilor de fer şi de mangan din apă, îndepărtarea mirosurilor şi gusturilor neplăcute, reducerea turbidităţii, a culorii, o puternică acţiune biocidă asupra bacteriilor, virusurilor, protozoarelor în contact scurt cu apa [37]. Dezinfecţia cu dioxid de clor este foarte apreciată pentru că posedă proprietăţi biocide, nu recţionează cu amoniacul din apă, nu generează halometani, nu prezintă toxicitate remanentă (fapt ce permite utilizarea în spitale, industria alimentară, piscicultură şi floricultură).
S-a introdus tratamentul preoxidativ cu dioxid de clor (ClO2), având proprietăţi superioare oxidative faţă de clorul gazos, cu avantajul major -cantitatea de halometani generaţi, presupuşi cancerigeni, în urma reacţiei cu apa au valori minime.
Oxidarea intermediară cu dioxid de clor conduce la modificarea parametrilor biologici ai apei, reducând prezenţa algelor şi a altor microorganisme acvatice. Totodată, oxidarea intermediară reduce substanţial cantitatea de Cl2 introdusă în compartimentul de apă potabilă la dezinfecţia finală.
Cl2+H2O → HOCl +HCl (3)
Acidul hipocloros este instabil si se descompune în oxigen activ şi acid clorhidric, conform reacţiei:
HOCl → HCl +O. (4)
Dezavantajul major a dezinfecţiei cu clor gazos o prezintă produşii secundari de reacţie din categoria trihalometanilor (THM), ce rezultăîn urma reacţiei clorului cu substanţele organice din apă, cloroform, diclorometan ( presupuşi a fi agenţi cancerigeni[13,27,33]).
Cloraminele pot fi utilizate în dezinfecţia apei potabile, având efect bactericid mai scăzut decât al clorului. La hiperclorare apar subproduşi de reacţie, precum halometanii, compuşi presupuşi periculoşi [13,34-35].
O alternativă la dezinfecţia cu clor gazos o constituie dioxidul de clor[36], care prezintăproprietăţi specifice: caracter puternic oxidant, capacitate de a reduce, până la eliminarea totalăa ionilor de fer şi de mangan din apă, îndepărtarea mirosurilor şi gusturilor neplăcute, reducerea turbidităţii, a culorii, o puternică acţiune biocidă asupra bacteriilor, virusurilor, protozoarelor în contact scurt cu apa [37]. Dezinfecţia cu dioxid de clor este foarte apreciată pentru că posedă proprietăţi biocide, nu recţionează cu amoniacul din apă, nu generează halometani, nu prezintă toxicitate remanentă (fapt ce permite utilizarea în spitale, industria alimentară, piscicultură şi floricultură).
S-a introdus tratamentul preoxidativ cu dioxid de clor (ClO2), având proprietăţi superioare oxidative faţă de clorul gazos, cu avantajul major -cantitatea de halometani generaţi, presupuşi cancerigeni, în urma reacţiei cu apa au valori minime.
Oxidarea intermediară cu dioxid de clor conduce la modificarea parametrilor biologici ai apei, reducând prezenţa algelor şi a altor microorganisme acvatice. Totodată, oxidarea intermediară reduce substanţial cantitatea de Cl2 introdusă în compartimentul de apă potabilă la dezinfecţia finală.
2.1.3.4.2. Dezinfecţia cu ozon
Ozonul este oxidantul cel mai puternic folosit pentru potabilizarea apei, principalul său avantaj fiind lipsa totală a produşilor secundari de reacţie specifici tratamentului cu clor [13]. Ozonul este preparat din aer uscat sau oxigen sub efectul radiaţiei ultraviolete sau a descărcărilor electrice de înaltă tensiune cuprinse între 4– 30 KV, conform reactiei chimice[38,18]:
3O2 ↔ 2O3 + 34.5cal/mol
3O2 ↔ 2O3 + 34.5cal/mol

Figura 12. Generatoare orizontale de ozon, Staţia de Tratare a Apei de la Santa Clara Valley USA
Ozonul este stabil numai la temperaturi foarte ridicate, iar la temperatură normală se descompune cu degajare de căldurăşi molecula de oxigen, eliberându-se al treilea atom de oxigen sub formă activă, conferind ozonului proprietăţi oxidante[13,38,39]:
O3 + H2O → 2HO∙ +O2 (5)
O3 + HO∙ → O2- ∙ + HO2∙ (6)
Tratarea cu ozon permite eliminarea unor germeni rezistenţi la alţi agenţi convenţionali de dezinfectie. Timpul de contact este scurt (cca. 4 minute), asigurând distrugerea în proporţie de 90% a microorganismelor contaminante.
O3 + H2O → 2HO∙ +O2 (5)
O3 + HO∙ → O2- ∙ + HO2∙ (6)
Tratarea cu ozon permite eliminarea unor germeni rezistenţi la alţi agenţi convenţionali de dezinfectie. Timpul de contact este scurt (cca. 4 minute), asigurând distrugerea în proporţie de 90% a microorganismelor contaminante.
2.1.3.4.3. Dezinfectanţi fizici
Radiaţiile cu o anumită lungime de undă au proprietăţi penetrante remarcabile, ceea ce le pretează pentru procesul de dezinfecţie, cele mai utilizate fiind radiaţiile ultraviolete, nucleare (în special cele gamma) şi câmpul de radiaţie ultrasonic [27].
2.1.3.4.3.1. Dezinfecţia cu radiaţii UV
Lungimea de undă a radiaţiei UV la care se manifestă efectul bactericid este cuprins între 2500 – 2800 Ǻ [27,40]. Radiaţia UV este capabilă să distrugă microorganismele, într-un mediu lipsit de oxigen, fără a fi implicat vreun proces chimic, acţiunea bactericidă manifestându-se prin efect distructiv la nivel de ADN şi ARN[41]. Apa supusă tratamentului prin iradiere, trebuie săîndeplinească anumite cerinţe: să circule cu viteză redusă, turbiditatea nu trebuie să depăşească 2-3° NTU, iar înălţimea apei în compartimentul de iradiere nu trebuie să depăşescă 15- 20 cm.
În figura 13 este prezentat dispozitivul de iradiere cu radiaţii UV, testat în staţia de tratare Şorogari din cadrul SC.Apavital SA[14].Sursa de radiaţie utilizată a fost o lampa de cuarţ cu descărcări în vapori de mercur.
În figura 13 este prezentat dispozitivul de iradiere cu radiaţii UV, testat în staţia de tratare Şorogari din cadrul SC.Apavital SA[14].Sursa de radiaţie utilizată a fost o lampa de cuarţ cu descărcări în vapori de mercur.

Figura 13. Dispozitiv de iradiere cu radiaţii UV, testat la Apavital SA Iasi
2.1.3.5.Reglarea pH-ului
În coloana de apă se face legătura cu rezervoarele cu reactivii de tratare(coagulantul, clorura ferică, dioxidul de clor, acidul clorhidric), cu un pH-metru şi un turbidimetru.

Figura 14. Cămin injecţie reactivi tratare
Aici se primesc informaţii referitor la apa brută ce intră în proces (turbiditate, pH), valori ce hotărăsc dozele de coagulant şi funcţionarea liniei de corecţie a pH-ului.
La contactul reactivilor cu apa începe practic procesul de tratare. La ieşire apa parcurge un mixer static subteran, pentru omogenizarea amestecului apă –reactivi.
Turbiditatea apei este dată de prezenţa în suspensie a unor particule coloidale, cu timp de decantare foarte mare. Aceste particule coloidale au încărcare electrostatică negativă. Ionul feric, Fe3+ din clorura ferică în soluţie apoasă este neutralizat de sarcinile negative a coloizilor, formând un miceliu, ce va creşte în dimensiune, pe parcursul avansării procesului de coagulare. În caz de necesitate, la apariţia unor unde de poluare, în camera de mixare se introduce pudră de cărbune activ, care va adsorbi componenta poluantă, iar produsul rezultat se va depune sub formă de slam pe fundul decantorului.
Flocoanele formate în urma coagulării, sunt tratate cu soluţia de polimer (solubil în apă) care are rolul unui adeziv, formându-se structuri de dimensiuni mari prin lipirea flocoanelor deja formate, astfel decantându-se mai uşor.
Toate echipamentele de dozare a reactivilor sunt dotate cu câte două pompe, una din ele obligatoriu de rezervă, toate fiind controlate prin convertizoare de frecvenţă, local sau de la distanţă de către computer. Toate echipamentele de dozare sunt dotate cu detectoare de pierderi, ce avertizează în timp util operatorul.
La contactul reactivilor cu apa începe practic procesul de tratare. La ieşire apa parcurge un mixer static subteran, pentru omogenizarea amestecului apă –reactivi.
Turbiditatea apei este dată de prezenţa în suspensie a unor particule coloidale, cu timp de decantare foarte mare. Aceste particule coloidale au încărcare electrostatică negativă. Ionul feric, Fe3+ din clorura ferică în soluţie apoasă este neutralizat de sarcinile negative a coloizilor, formând un miceliu, ce va creşte în dimensiune, pe parcursul avansării procesului de coagulare. În caz de necesitate, la apariţia unor unde de poluare, în camera de mixare se introduce pudră de cărbune activ, care va adsorbi componenta poluantă, iar produsul rezultat se va depune sub formă de slam pe fundul decantorului.
Flocoanele formate în urma coagulării, sunt tratate cu soluţia de polimer (solubil în apă) care are rolul unui adeziv, formându-se structuri de dimensiuni mari prin lipirea flocoanelor deja formate, astfel decantându-se mai uşor.
Toate echipamentele de dozare a reactivilor sunt dotate cu câte două pompe, una din ele obligatoriu de rezervă, toate fiind controlate prin convertizoare de frecvenţă, local sau de la distanţă de către computer. Toate echipamentele de dozare sunt dotate cu detectoare de pierderi, ce avertizează în timp util operatorul.

Figura 14. Sistemul de dozare cu clorura ferică

Figura 15. Sistemul de dozare a polimerului

Figura 16. Sistem preparare şi dozare lapte de var

Figura 17. Generatorul de dioxid de clor

Figura 18. Sistemul de dozare dioxid de clor

Figura 19. Sala containerelor de clor

Figura 20. Dispozitivele de clorare
Staţia de dezinfecţie adăposteşte linia de generare a dioxidului de clor, clorinatoarele, sala de depozitare a containerelor de clor. Linia de generare a dioxidului de clor este complet automatizată, fiind protejată de senzori de măsură a emisiilor de gaz, debite, presiuni, ce pot opri dispozitivul în caz de depăşiri periculoase, sistemul de alarmare în caz de emisie chimică fiind atât vizual (prin lumini), cât şi acustic.
Apa potabilă acumulată în rezervor este preluată şi trimisă prin sistemul de pompare în reţeaua de distribuţie a oraşului.
Principalul indicator de calitate îmbunătăţit este valoarea turbidităţii, datorită procesului de coagulare /floculare. Înlocuirea sulfatului de aluminiu cu clorura ferică este, de asemenea, un factor pozitiv în caliatea apei potabile. O realizare de mare importanţă este introducerea treptei de filtrare pe cărbune activ, cât şi oxidarea cu dioxid de clor (reduc cu o eficienţă de 80% încărcarea organică din apă, eliminând totodată complet fitoplanctonul din apa brută, în care se află câteva sute de mii entităţi pe litru, astfel încât în apa din rezervor nemaiexistând alge).
În figura 21 este redată schema bloc a circuitului apei în municipiului Iaşi[11, 12]: sistemul de captare apă brută, transport, tratare, distribuţie, canalizare, epurare ape reziduale, deversare în emisar.
Apa potabilă acumulată în rezervor este preluată şi trimisă prin sistemul de pompare în reţeaua de distribuţie a oraşului.
Principalul indicator de calitate îmbunătăţit este valoarea turbidităţii, datorită procesului de coagulare /floculare. Înlocuirea sulfatului de aluminiu cu clorura ferică este, de asemenea, un factor pozitiv în caliatea apei potabile. O realizare de mare importanţă este introducerea treptei de filtrare pe cărbune activ, cât şi oxidarea cu dioxid de clor (reduc cu o eficienţă de 80% încărcarea organică din apă, eliminând totodată complet fitoplanctonul din apa brută, în care se află câteva sute de mii entităţi pe litru, astfel încât în apa din rezervor nemaiexistând alge).
În figura 21 este redată schema bloc a circuitului apei în municipiului Iaşi[11, 12]: sistemul de captare apă brută, transport, tratare, distribuţie, canalizare, epurare ape reziduale, deversare în emisar.
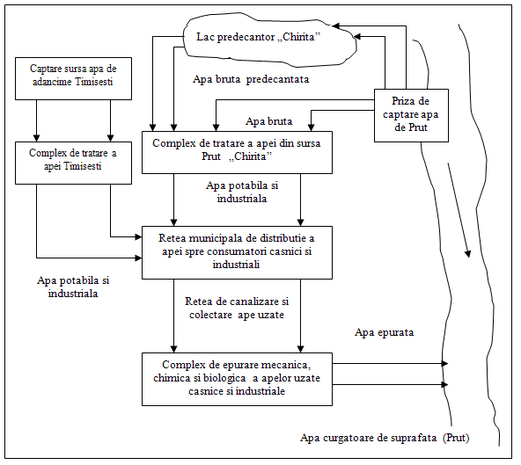
Figura 21. Schema bloc a circuitului apei în sistem centralizat (specific municipiului Iaşi)
Alimentarea cu apă a municipiului Iaşi se realizează din două surse: subterană (fronturile de captare cu puţuri de la Timişeşti) şi de suprafaţă - râul Prut. Pentru municipiul Iaşi s-a ales acest sistem mixt pentru a putea asigura debitele şi presiunile de serviciu necesare unei bune desfăşurări a activităţilor socio-economice. Avantajul major al acestui sistem mixt constă în posibilitatea de a prelua alimentarea generală cu apa de la una din surse în cazul când cealaltă este oprită sau se află în regim de avarie. Alimentarea din surse de suprafaţă se realizează cu apa din râul Prut şi lacul predecantor Chiriţa. Procesul de tratare a apei brute de suprafaţă se desfăşoară în Complexul de Tratare a Apei „Chiriţa”. Se observă că apa brută din râul Prut este captată cu un sistem de pompe ce constituie priza de captare. Apa este directionată prin magistralele de transport, spre lacul Chiriţa, fie spre Complexul de Tratare Chiriţa. Lacul Chiriţa este utilizat ca un predecantor natural de mare capacitate(aproximativ 5 milioane de m3 apă). Apa predecantată utilizată în procesul de tratare prezintă avantajul unei turbidităţi mici, ceea ce implică costuri moderate de tratare. Apa predecantată se utilizează în momentul când apa râului Prut prezintă încărcare suspensională mare, ceea ce implică costuri de producţie ridicate. Alimentarea cu apă din surse de adâncime se realizează cu ajutorul frontului de captare cu puţuri de la Timişeşti. Apa de adâncime având caracteristici fizico-chimice superioare celei de suprafaţă (Prut, lac predecantor Chiriţa), nu necesită procese specifice de tratare fiind suficiente operaţiunile de clorare şi post-clorare pe parcursul magistralei de transport (statia Săbăoani, Târgu Frumos, complexul Aurora).
2.2. Realizări proprii
Pentru a înţelege mai bine procesul tehnologic, am realizat o vizită de lucru la furnizorul de apă potabilă din Iaşi, APAVITAL SA.
Astfel, înţelegând procedura industrială de potabilizare a apei brute, am conceput o schemă în miniatură, adaptând/ modificând o parte din etape.
Astfel, înţelegând procedura industrială de potabilizare a apei brute, am conceput o schemă în miniatură, adaptând/ modificând o parte din etape.
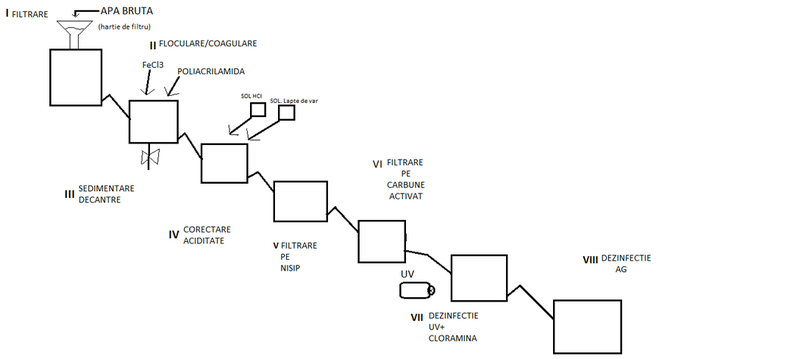
Figura 22. Schema bloc a instalației de potabilizare a apei brute construită de echipa APA
2.2.1. Materiale şi ustensile
Ustensile: panou OSB, şuruburi cu piuliţe 3 dimensiuni, suport susţinere, 3 vase mari cu capac, 4 vase mici cu capac, pâlnie, hârtie de filtru, paie, tuburi silicon, 4 seringi, cutie dulciuri, cutie plastilină, cutie desen, cutie medicamente, led UV, baterie, întrerupător, conductor, grafit, mixer coctail, pipetă, scotch dublu adeziv, etichete, adeziv poxipol, vată, clame de hârtie,coliere din plastic,
Reactivi: apă brută, soluţie FeCl3, poliacrilamidă, soluţie HCl, lapte de var, nisip cuarţos, cărbune activat, cloramină, argint.
Reactivi: apă brută, soluţie FeCl3, poliacrilamidă, soluţie HCl, lapte de var, nisip cuarţos, cărbune activat, cloramină, argint.
2.2.2. Mod de lucru
Pentru a realiza instalaţia, am ales un suport de susţinere, de care am prins panoul OSB cu 2 şuruburi.
Am căutat recipiente cu scopul de a construi camerele de reacţie. Pentru a putea fi prinse pe panoul instalaţiei, am ales recipiente din plastic cu capac, de 2 dimensiuni. Legătura între recipiente a fost realizată cu paie de suc sau cu tuburi din silicon. Pentru o mai bună etanşare, am acoperit îmbinările cu adeziv poxipol. Ca robinet, am folosit clame de hârtie, care opturează tuburile. La captătul de ieşire a fiecărui pai am pus dop din vată pentru a nu curge eventuale părţi solide. La ieşirile,,conductelor” din paie am îndoit racordurile pentru ca doar apa să treacă prin acestea.
I. Filtrarea primară a apei brute, pentru îndepărtarea impurităţilor grosiere se face printr-o pâlnie cu hârtie de filtru. Pentru aerisire, s-a conectat la pâlnie un tub suplimentar. Trecerea în a doua cameră se realizează prin cădere.
II.-III. În camera de floculare/ coagulare/ sedimentare/ decantare, care este izolată de următoarea cameră prin intermediul unui robinet (clamă de hârtie) se adaugă FeCl3, sub agitare (cu mixerul pentru coctail imobilizat de panou), care are ca rol de a interacţiona cu particulele mici aflate în suspensie în apă. Ionii Fe3+ din clorura ferică în soluţie apoasă interacţionează cu particulele coloidale de sarcină negativă formând miceliu sau flocoane. Astfel, este diminuată turbiditatea apei. Se opreşte agitarea şi se adaugă polimer (cu rol de adeziv), formându-se structuri de dimensiuni mari prin lipirea flocoanelor deja formate, astfel decantându-se mai uşor. Se aşteaptă aproximativ 30 minute până se decantează (se deschide clama) pentru ca apa să treactă în următorul compartiment. Tubul de legătură la ieşire este cuplat pe o poziţie superioară celorlalte, pentru a lăsa loc sedimentelor.
După traversarea a10-15 L apă, se evacuează sedimentele prin partea inferioară a recipientului, prin absorbţie cu ajutorul unei seringi.
IV. Apa ajunsă în camera IV este testată din punct de vedere al pH-ului. Se utilizează pipeta, luându-se 5 ml probă şi se utilizează pH-metrul mobil. De regulă, apa are pH slab bazic (pH~8). Se conectează la rezervorul cu soluţie de HCl (seringă) şi se adaugă soluţia. Se verifică din nou pH-ul. Dacă ajunge la valoarea de 5,5 este în regulă. Dacă se scapă prea mult HCl sau eventual, apa este accidental poluată cu acizi, se utilizează lapte de var din recipientul vecin.
Prelevarea probelor se face într-un vas cu 2 compartimente (vas de spălare pensoane).
II.-III. În camera de floculare/ coagulare/ sedimentare/ decantare, care este izolată de următoarea cameră prin intermediul unui robinet (clamă de hârtie) se adaugă FeCl3, sub agitare (cu mixerul pentru coctail imobilizat de panou), care are ca rol de a interacţiona cu particulele mici aflate în suspensie în apă. Ionii Fe3+ din clorura ferică în soluţie apoasă interacţionează cu particulele coloidale de sarcină negativă formând miceliu sau flocoane. Astfel, este diminuată turbiditatea apei. Se opreşte agitarea şi se adaugă polimer (cu rol de adeziv), formându-se structuri de dimensiuni mari prin lipirea flocoanelor deja formate, astfel decantându-se mai uşor. Se aşteaptă aproximativ 30 minute până se decantează (se deschide clama) pentru ca apa să treactă în următorul compartiment. Tubul de legătură la ieşire este cuplat pe o poziţie superioară celorlalte, pentru a lăsa loc sedimentelor.
După traversarea a10-15 L apă, se evacuează sedimentele prin partea inferioară a recipientului, prin absorbţie cu ajutorul unei seringi.
IV. Apa ajunsă în camera IV este testată din punct de vedere al pH-ului. Se utilizează pipeta, luându-se 5 ml probă şi se utilizează pH-metrul mobil. De regulă, apa are pH slab bazic (pH~8). Se conectează la rezervorul cu soluţie de HCl (seringă) şi se adaugă soluţia. Se verifică din nou pH-ul. Dacă ajunge la valoarea de 5,5 este în regulă. Dacă se scapă prea mult HCl sau eventual, apa este accidental poluată cu acizi, se utilizează lapte de var din recipientul vecin.
Prelevarea probelor se face într-un vas cu 2 compartimente (vas de spălare pensoane).
V. Filtrarea se face pe nisip cuarţos, recipientul fiind umplut aproximativ o treime cu acest material filtrant. Tubul(paiul) este introdus la nivelul nisipului, având un dop de vată şi, suplimentar, pentru a nu curge şi nisipul odată cu apa paiul este ridicat la partea flexibilă.
VI. Filtrarea continuă în următorul recipient pe cărbune activat sub formă de granule (obţinut din lemn (mangal), lignit, turbă şi deşeuri petroliere carbonizate lent în absenţa aerului şi activate prin injectarea de gaze oxidante la temperaturi foarte înalte). Această filtrare are ca scop principal corectarea proprietăţilor organoleptice ale apei (gust, culoare, miros, reţinerea ultimilor poluanţi chimici). La interfaţa de separaţie apă-suprafaţa granulei se creează o membrană microbiologică, în care se desfăşoară fenomenele de adsorbţie biochimică a substanţelor cu risc (pesticide, derivaţi fenolici, combustibili petrolieri, reziduuri petroliere, etc.).
VI. Filtrarea continuă în următorul recipient pe cărbune activat sub formă de granule (obţinut din lemn (mangal), lignit, turbă şi deşeuri petroliere carbonizate lent în absenţa aerului şi activate prin injectarea de gaze oxidante la temperaturi foarte înalte). Această filtrare are ca scop principal corectarea proprietăţilor organoleptice ale apei (gust, culoare, miros, reţinerea ultimilor poluanţi chimici). La interfaţa de separaţie apă-suprafaţa granulei se creează o membrană microbiologică, în care se desfăşoară fenomenele de adsorbţie biochimică a substanţelor cu risc (pesticide, derivaţi fenolici, combustibili petrolieri, reziduuri petroliere, etc.).
VII. Dezinfecţia din camera VII se realizează în două faze: iradiere cu raze ultraviolete şi traterea cu cloramină.
În ţara noastră legea obligă la realizarea dezinfecţiei cu compuşi ai clorului. Tratarea cu clor gazos duce la compuşi nocivi, iar în instalaţia noastra ar fi riscant deoarece acesta este un gaz iritant. Eficientă este folosirea dioxidului de clor, care nu conduce la produşi secundari toxici, dareste foarte instabil, fiind exploziv. Astfel, am ales varianta mai sigură din punct de vedere a instalaţiei, şi anume utilizarea pastilelor de cloramină. Alături este rezervat o încăpere (cutie de la plastilină) cu pastile de cloramină.
În multe alte ţări, clorinarea este exclusă, dezinfecţia realizându-se prin metode moderne, cum ar fi ozonarea sau iradierea cu raze UV. Noi ma reuşit să realizăm un dispozitiv de iradiere cu raze ultraviolete (cutie medicamente, conductor, led UV, întrerupător şi rezistenţă o bucată de mină de grafit). Apa supusă tratamentului prin iradiere circulă cu viteză redusă, iar înălţimea acesteia în compartimentul de iradiere nu depăşeste 20 cm.
În ţara noastră legea obligă la realizarea dezinfecţiei cu compuşi ai clorului. Tratarea cu clor gazos duce la compuşi nocivi, iar în instalaţia noastra ar fi riscant deoarece acesta este un gaz iritant. Eficientă este folosirea dioxidului de clor, care nu conduce la produşi secundari toxici, dareste foarte instabil, fiind exploziv. Astfel, am ales varianta mai sigură din punct de vedere a instalaţiei, şi anume utilizarea pastilelor de cloramină. Alături este rezervat o încăpere (cutie de la plastilină) cu pastile de cloramină.
În multe alte ţări, clorinarea este exclusă, dezinfecţia realizându-se prin metode moderne, cum ar fi ozonarea sau iradierea cu raze UV. Noi ma reuşit să realizăm un dispozitiv de iradiere cu raze ultraviolete (cutie medicamente, conductor, led UV, întrerupător şi rezistenţă o bucată de mină de grafit). Apa supusă tratamentului prin iradiere circulă cu viteză redusă, iar înălţimea acesteia în compartimentul de iradiere nu depăşeste 20 cm.
VIII. În ultima cameră apa este depozitată, fiind potabilă. Considerăm că şi aici are loc dezinfecţia în timp, deoarece am adăugat o monedă de argint, care are rol de a distruge microorganismele.
Apa păstrată în vase de argint are calităţile unui antibiotic extrem de eficient, iar utilizarea tacâmurilor de argint are acelaşi rol. De asemeni, o monedă de argint aruncată în fântână, în afara ,,îndeplinirii unei dorinţe”, are rol dezinfectant.
Apa păstrată în vase de argint are calităţile unui antibiotic extrem de eficient, iar utilizarea tacâmurilor de argint are acelaşi rol. De asemeni, o monedă de argint aruncată în fântână, în afara ,,îndeplinirii unei dorinţe”, are rol dezinfectant.
2.3. Concluzii
1. Am realizat documentarea despre etapele potabilizării apei brute.
2. Am identificat materialele, ustensilele necesare şi am făcut un plan care a ridicat diverse probleme, dar care au fost rezolvate folosind cunoştinţe de chimie, fizică, biologie, educaţie tehnologică şi TIC.
3. Am obţinut o miniatură a unei instalaţii de potabilizare a apei brute.
4. Am înlocuit cu clorura ferică (FeCl3) a sulfatului de aluminiu (Al2(SO4)3, acesta fiind implicat în declanşarea sindromului Allzenheimer.
5. În locul tratamentului preoxidativ cu dioxid de clor (ClO2), am folosit pasile de cloramină
6. Am introdus un agent floculant- un polimer poliacril-amidă în scopul formării unor sisteme floculare ferme şi de dimensiune mari, uşor decantabile.
2. Am identificat materialele, ustensilele necesare şi am făcut un plan care a ridicat diverse probleme, dar care au fost rezolvate folosind cunoştinţe de chimie, fizică, biologie, educaţie tehnologică şi TIC.
3. Am obţinut o miniatură a unei instalaţii de potabilizare a apei brute.
4. Am înlocuit cu clorura ferică (FeCl3) a sulfatului de aluminiu (Al2(SO4)3, acesta fiind implicat în declanşarea sindromului Allzenheimer.
5. În locul tratamentului preoxidativ cu dioxid de clor (ClO2), am folosit pasile de cloramină
6. Am introdus un agent floculant- un polimer poliacril-amidă în scopul formării unor sisteme floculare ferme şi de dimensiune mari, uşor decantabile.